UVECO
Induction
of microbial community responses and dissolved organic matter transformations
by UltraViolet radiation in marine ECOsytems
| I. INT…R T SCIENTIFIQUE | |
| > Le rayonnement ultraviolet dans le milieu marin | |
| > Les dommages causťs par le rayonnement UV aux organismes planctoniques | |
|
> Les
processus de photoaltťration de la matiŤre organique dissoute |
|
| > Impact du rayonnement UV sur les processus de dťgradation biologique et photochimique des composťs soufrťs du type DMS et DMSP | |
| 2. OBJECTIFS DU PROJET UVECO (click to go..) | |
| Sites d'ťtude retenus dans le projet UVECO (click to go to ..) | |
|
|
|
|
Le rayonnement solaire produit un large spectre de
radiations dont une partie correspond ŗ des radiations ultraviolettes
(UV) dont les longueurs d’ondes sont comprises entre 200 et
400 nm. Le rayonnement UV-C, compris entre 200 et 280 nm, est efficacement
absorbť par l’atmosphŤre et n'atteint pas la surface de la
terre. Le rayonnement UV-B, compris entre 280 et 320 nm, est fortement
absorbť par l’ozone de la stratosphŤre et donc partiellement ťliminť des
radiations atteignant la surface de la terre (Fig. 1). Cependant,
les UV-B rťsiduels (principalement entre 300 et 320 nm) peuvent induire
des effets prononcťs sur les organismes vivants et la matiŤre organique
dťtritique. Le rayonnement UV-A, compris entre 320 et 400 nm, est
trŤs peu absorbť par l’atmosphŤre et atteint la surface de
la terre sans attťnuation. Ce dernier, comme le rayonnement visible
(400-700 nm), est attťnuť par la charge en aťrosols de l'atmosphŤre
et la nťbulositť (Fig. 1).
Le flux d'UV-B atteignant la surface de la terre constitue
l'une des variables physiques susceptibles d'Ítre modifiťe dans
l'avenir en raison des changements climatiques d'origine anthropique
ou naturelle. L'un des facteurs majeurs responsables de l'augmentation
du flux d'UV-B rťsulte de la diminution de la couche d'ozone liťe
au rejet dans l'atmosphŤre de composťs chimiques destructeurs d'ozone
comme les chlorofluorocarbones (CFC). Ce phťnomŤne a atteint une
dimension considťrable en Antarctique, mais il touche ťgalement
dans une moindre mesure l'Arctique et des latitudes moyennes des
deux hťmisphŤre ŗ certaines pťriodes de l'annťe (Hofmann et Deshler,
1991 ; McKenzie et al., 1999). Un rapport rťcent (1) indique
que les dispositions prises en matiŤre de rťduction des ťmissions
de CFC semblent efficaces (mÍme si un trou d'ozone d'une ampleur
jamais ťgalťe a ťtť enregistrť en 2000 en Antarcticque; Angell
et al., 2000), et que le problŤme pourrait Ítre rťsolu dans les
prochaines dťcennies. Cependant, ce rapport indique ťgalement que
si le rayonnement UV (UV-R) a pu augmenter de l'ordre de 10% dans
certaines rťgions, la diminution de la couche d'ozone n'est pas
le seul facteur explicatif. Des modifications de l'albedo de surface,
de la couverture nuageuse, des aťrosols de la troposphŤre peuvent ťgalement
influer ŗ grande ťchelle sur le flux d'UV atteignant la surface
du globe. La nťbulositť et la quantitť d’aťrosols sont susceptibles
de variations significatives dans les prochaines annťes du fait
de la combustion des fuels fossiles (et de la production concomitante
de composťs organiques solubles en phase aqueuse qui peuvent agir
comme noyaux de condensation) et du changement global de climat
(et de l’ťmission probable de DMS pouvant produire in
fine des sulfates et des noyaux de condensation). Ces deux
paramŤtres ťtant ťtroitement liťs au changement global, des travaux
futurs devraient permettre d’ťvaluer leurs effets sur le
rayonnement UV ŗ la surface de l’ocťan (Moran et Zepp, 2000).
Dans la colonne d’eau, la pťnťtration des UV-R
est contrŰlťe par le coefficient d’attťnuation diffuse Kd,
qui correspond ŗ la transmittance de la lumiŤre solaire dans l’eau
de mer (Jerlov, 1976 ; Sogandares et Fry, 1997). Les valeurs
de Kd indiquent que les UV-R de plus courtes longueurs d’ondes
sont attťnuťs plus rapidement et que le degrť d’attťnuation
dťcroÓt du domaine UV vers le domaine visible (Smith et Baker,
1979). Par exemple, en Atlantique tropicale, les profondeurs du
10% du flux d’UV de surface sont respectivement de 25, 35
et 60 m ŗ 320, 340 et 380 nm (Herndl et al., 1998). Nťanmoins,
le Kd ne varie pas seulement avec la longueur d’onde :
il peut varier en fonction du type d’environnement marin
considťrť (Smith et Baker, 1979 ; Moran et Zepp, 2000). En
effet, le coefficient d’absorption des UV dans les eaux naturelles
dťpend fortement des concentrations en matiŤre organique dissoute
(MOD), en substances jaunes dissoutes (MOD chromophorique), en
dťtritus et matťriel particulaires et en biomasse phytoplanctonique
(Smith et Baker, 1979 ; Kirk, 1994b ; Moris et al., 1995 ;
Nelson et Guarda 1995 ; Siegel et Michaelis, 1996 ; Sommuraga
et Psenner, 1997 ; Stambler et al., 1997 ; Smith et al.,
1999). Le coefficient d’absorption de la MOD est trŤs faible
en fin du domaine visible (dans le rouge) et augmente exponentiellement
avec la diminution de la longueur d’onde dans le domaine
UV. Les systŤmes marins cŰtiers sont donc caractťrisťs par un Kd ťlevť tandis
que les eaux pťlagiques possŤdent un Kd beaucoup plus faible. Les
profondeurs de 1% du flux UV de surface ŗ 320 nm sont pour des
systŤmes cŰtiers et pťlagiques typiques respectivement de 6,8 et
de 49 m (Moran et Zepp, 2000). La MOD chromophorique contribue
majoritairement ŗ l’absorption des UV-R dans l’ocťan,
en particulier dans les rťgions cŰtiŤres (Kirk, 1994b ; DeGrandpre
et al., 1996) mais ťgalement dans les eaux oligotrophes (Siegel
et Michaelis, 1996). Cependant les travaux prťliminaires de Vasilkov
(2001), ont indiquť que la Mťditerranťe apparaÓt comme une zone
relativement exposťe aux UV-R avec un ťclairement UV de surface
(moyennť sur 5 jours) de 8 kJ.m-2 (l : 290 ŗ 400 nm) et une profondeur du 10 %
du flux UV-R de surface de 17 m. De nombreux ťcosystŤmes aquatiques marins et d’eaux
douces sont donc susceptibles d’Ítre exposťs ŗ une augmentation
(ou ŗ une diminution) des flux d'UV-B au cours des prochaines annťes.
Il est donc important de continuer ŗ ťvaluer les effets des UV-R
sur les ťcosystŤmes aquatiques afin de prťdire l’impact d’une ťventuelle
modification du flux d'UV ŗ la surface des ocťans.
|
|
|
|
Parmi
les diffťrents dommages causťs par le rayonnement solaire, ceux
causťs ŗ l’ADN sont les plus importants. L’absorption
directe de photons UV-B par l’ADN entraÓne la formation de
liaisons entre des bases pyrimidines adjacentes qui bloquent l’ADN
polymťrase et les enzymes de reverse transcriptase. Les UV-A et
la lumiŤre visible (400 ŗ 700 nm; PAR) entraÓnent quant ŗ eux des
dommages indirects qui rťsultent de l’absorption de photons
de ces bandes spectrales par diffťrents chromophores (e.g., NADH,
NADPH, flavines, protťines). Ces molťcules peuvent alors transfťrer
leur ťnergie ŗ l'ADN et l'endommager ou conduire ŗ la formation
d'espŤces d'oxygŤne rťactifs, dommageables pour l'ADN, les protťines
et les lipides. Les dommages directs ou indirects causťs ŗ l'ADN
conduisent aux mÍmes effets avec un blocage de l'activitť de synthŤse
et de division. Une rťparation incomplŤte de ces dommages peut
conduire ŗ la mort cellulaire ou ŗ l'apparition de mutations. Le
rayonnement UV et visible entraÓne ťgalement une multitude d’autres
effets, principalement au niveau des membranes dont la plupart
sont "sublťtaux" (e.g., altťration de la permťabilitť membranaire,
du transport actif, de la chaÓne de transport d'ťlectron, ou du
gradient ťlectrochimique transmembranaire). Ces dommages peuvent
affecter la croissance et la division cellulaire et agir en synergie
avec les dommages causťs ŗ l’ADN pour augmenter la lťtalitť (Fig.
2).
Les
rťponses du phytoplancton ŗ l'intensitť lumineuse visible reÁue
sont nombreuses et complexes (mťtaboliques, physiologiques). Le
rayonnement UV a ťgalement un impact important sur ces organismes
qu'il est important de bien apprťhender mais surtout de bien diffťrencier
des effets induits par le PAR qui peuvent au final se traduire
par le mÍme type d'effet (production de pigments photoprotecteurs,
croissance rťduite, production primaire inhibťe, photodťgradation
de certains composants cellulaires) mais engendrť par des mťcanismes
physiologiques totalement diffťrents. Le rayonnement UV peut induire
une baisse significative de la production primaire, qui a pu Ítre
mesurťe jusqu'ŗ une profondeur de 20 m en Antarctique durant un ťvťnement
de trou d'ozone (Smith et al., 1992). Ces effets se traduisent ťgalement
par une diminution importante des valeurs des paramŤtres photosynthťtiques
du phytoplancton (Behrenfeld et al., 1995 ; Hšder et al., 1998)
et par une augmentation importante de l'excrťtion de photoproduits
dans le milieu extracellulaire (Pausz et Herndl, 1999). Il faut
noter que l'inhibition de la production primaire n’est pas
nťcessairement accompagnťe d’une variation significative
des concentrations en chlorophylle ou des composťs photoprotecteurs
(Vinebrooke et Leavitt, 1998). Par ailleurs, il est connu que la
sensibilitť du phytoplancton vis-ŗ-vis du rayonnement UV varie
en fonction des espŤces (Karentz et al., 1991; Wšngberg et al.,
1996). Bien qu’aucune ťtude ne l'ait clairement ťtabli pour
le milieu marin, il est vraisemblable que cette sensibilitť est
plus importante pour les petites classes de taille, notamment les
picocyanobactťries (Prochlorococcus et Synechococcus),
du fait que leur gťnome ne prťsente qu'une faible redondance de
gŤnes ce qui accroÓt
[FP1]
l'impact
des mutations. L’ťtude par cytomťtrie en flux du cycle
cellulaire de Prochlorococcus dans le milieu naturel
a suggťrť que cet organisme pourrait rťsister aux effets
nťfastes des UV-R sur l’ADN en surface en dťcalant
de plusieurs heures le dťbut de la phase de synthŤse de ce
composť par rapport aux populations plus profondes (Vaulot
et al., 1995).
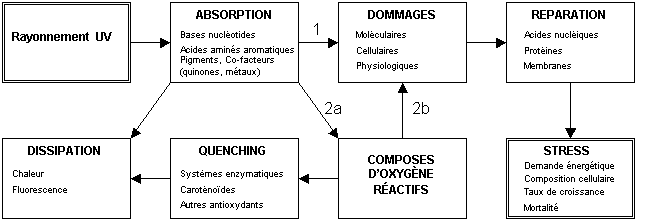
Fig. 2. Les
diffťrentes ťtapes qui conduisent au stress cellulaire ŗ partir
de l'exposition au rayonnement UV. Les dommages peuvent Ítre occasionnťs
directement par la dťgradation photochimique de biomolťcules (chemin
1) ou indirectement via la production de composťs d'oxygŤne
rťactifs (chemin 2a), qui peuvent alors causer des dommages plus
gťnťraux ŗ l'intťrieur de la cellule (chemin 2b). Le stress se
manifeste en termes d'augmentation de la demande ťnergťtique liťe
aux mťcanismes de protection et de rťparation mis en place; de
modifications dans la composition cellulaire (e.g., contenu lipidique),
qui peut affecter la qualitť nutritionelle des cellules pour les
maillons trophiques supťrieurs; de baisse du taux de croissance
rťsultant des dommages photochimiques et de l'augmentation de la
demande ťnergťtique (diminution du rendement de croissance); et,
aprŤs une exposition importante, d'une augmentation de la mortalitť.
Les bactťries hťtťrotrophes sont ťgalement particuliŤrement
exposťes au stress UV-R, car en plus de leur petite taille et leur
faible redondance gťnique, la plupart d’entre elles (ŗ l’exception
des bactťries photosynthťtiques non-oxygťniques) ne sont pas capables
[FP2]
de photoprotection
par des chromophores (Garcia-Pichel, 1994). Diffťrentes ťtudes
ont fait la preuve que les UV-R avaient un effet inhibiteur
sur diffťrentes fonctions physiologiques des bactťries marines
(activitťs de synthŤse, de division, exoenzymatiques, …)
(Miller et al., 1999), mÍme si, comme pour le phytoplancton,
les bactťries marines prťsentent une certaine diversitť de
rťsistance au stress UV-R (Joux et al., 1999; Arietta et
al., 2001). Il a ťtť montrť que les UV-R pouvaient rťduire
de 40 ŗ 70% l'activitť bactťrienne en surface (Herndl et
al., 1993; Aas et al., 1996; Sommaruga et al., 1997; Joux
et al., donnťes non publiťes [travaux du PNEC ART5]). Afin
de rťparer ces dommages, les bactťries sont capables de mettre
en place des mťcanismes de rťparation ŗ la lumiŤre (photorťactivation
par les UV-A et la lumiŤre visible plus en profondeur) ou ŗ l'obscuritť (recombinaison/excision).
Les UV-R pourraient donc modifier la distribution spatiale
(en fonction de la profondeur) et temporelle (cycle jour/nuit)
de l'activitť bactťrienne hťtťrotrophe. Les UV-R pourraient ťgalement
modifier les voies biogťochimiques de transformation de l'azote,
du phosphore et du soufre, du fait de la sensibilitť de certaines
espŤces bactťriennes impliquťes dans le cycle de ces ťlťments
(Jeffrey et al., 2000).
|
|
Des hypothŤses rťcentes attribuent une place
grandissante au rŰle des rťactions photochimiques sur l'accessibilitť et
la biodťgradabilitť de la MOD par les bactťries (Bano et al., 1998 ;
Benner, 1998). De larges modifications des molťcules organiques comme
les acides gras et certains composťs carbonylťs comme les acides dicarboxyliques,
les cťtoacides ou les composťs dicarbonylťs ont dťjŗ ťtť observťes
dans l’atmosphŤre du fait de rťactions directement ou indirectement
liťes aux processus de photo-oxydation (Kawamura et Gagosian, 1987;
Sempťrť et Kawamura, soumis, et rťfťrences internes). Il est important
de noter que ces molťcules interviennent dans le cycle de respiration
des organismes hťtťrotrophes et seraient abondamment prťsentes dans
les couches supťrieures de l’Ocťan (Steinberg et Bada, 1984). Cependant,
du fait des difficultťs analytiques liťes ŗ la matrice saline, peu
de travaux se sont concentrťs sur l’ťtude de ces composťs. Cependant, des travaux indiquent que la rťponse
du bactťrioplancton en prťsence de MOD exposťe aux UV est fonction
de l’origine et certainement de la composition de la MOD avant exposition ŗ ce
rayonnement (Naganuma et al., 1996 ; Obernosterer et al., 2001).
Initialement labile, du matťriel pourrait devenir plus rťfractaire ŗ la
dťgradation biologique et Ítre ŗ l’origine de la formation de composťs
oxydants dommageables pour les organismes (Xenopoulos et Bird, 1997).
Inversement, certains composťs rťfractaires deviendraient facilement
utilisables par les organismes de la boucle microbienne (production
d’acides organiques de faible poids molťculaire, de composťs azotťs
comme l’ammonium, d’acides aminťs libres et de phosphate). Concernant
les transformations de la MOD sous l'effet des rayonnements UV, quelques
travaux ont portť sur la production de composťs carbonyles (Zhou et
Mopper 1997). D'autres ťtudes (Goes et al., 1996) se sont ťgalement
intťressťes aux consťquences du rayonnement UV naturel sur la distribution
molťculaire des sucres et des acides aminťs qui rťsultent en partie
de la dťgradation de polysaccharides ou de protťines. Bien que certaines
de ces molťcules comme les sucres n’absorbent pas directement les UV-R,
nos travaux prťliminaires rťalisťs dans le cadre du PNEC ART5 (Tedetti,
2002), indiquent clairement que la photolyse UV des nitrates peut induire
une production de photosensibilisateurs comme les radicaux OH..
Ces radicaux pouraient modifier la structure molťculaire des sucres
ou des acides gras et produire des molťcules ŗ faible poids molťculaire
facilement assimilables par les bactťries. L'effet d'une modification
de la distribution molťculaire des sucres, des composťs carbonylťs
et des acides aminťs sur l'assimilation bactťrienne suite ŗ une exposition
aux rayonnements UV reste encore relativement inexplorť. Plus de 80% de
la DOM formťe en milieu marin sont minťralisťs par les bactťries marines
(Del Giorgio et al., 1997) dont 15% dans la couche de surface ocťanique
(Bianchi et al., 1999) soumise aux ťchanges gazeux air-mer et au rayonnement
ultraviolet. Les facteurs contrŰlant le rendement de croissance des
bactťries (rapport du carbone transformť en biomasse sur le carbone
organique ingťrť) apparaissent comme relatifs aux conditions environnementales
et physiologiques ainsi qu’ŗ la qualitť du substrat. Par exemple, la
photodťgradation de la DOM produit des composťs ŗ faible poids molťculaire
qui sont gťnťralement plus oxydťs que les molťcules prťcurseurs. Ces
molťcules oxydťes tels les acides organiques ŗ faible poids molťculaire,
sont utilisťes avec moins d’efficacitť par les bactťries que des substrats
riches en ťnergie. Des rťsultats prťliminaires indiquent une modification
de l’ampleur de la respiration bactťrienne suivant l’intensitť des
UV-R. De la mÍme maniŤre, les dommages cellulaires des bactťries peuvent
modifier les capacitťs minťralisatrices des bactťries (Aas et al.,
1996 ; Miller, 2000).
L'oxydation photochimique directe de la matiŤre organique
dissoute colorťe (CDOM) en carbone inorganique dissous est ťgalement
un processus important ŗ prendre en considťration. La photooxydation
chimique de la CDOM dans les zones cŰtiŤres pourrait ainsi expliquer
le puits de carbone organique dissous d'origine terrestre (Johannessen
et Miller, 2001). Dans le milieu ocťanique, ce processus n'a jamais ťtť quantifiť de
maniŤre prťcise, mais on suppose qu'il pourrait constituer un puits
important pour la MOD produite in situ (Mopper et al., 1991).
Compte tenu des fortes variations saisonniŤres et
inter annuelles du flux de photons et des teneurs en MOD dans la couche
superficielle ocťanique, il est important de prťciser les processus
photochimiques de maniŤre qualitative et quantitative. C’est en effet
pendant la pťriode de plus fort rayonnement (mai-juillet) que se trouvent
associťes une forte production primaire avec une production et une
accumulation de MOD dans les eaux de surface (Blight et al., 1995 ;
Williams 1995). |
|
|
|
L'impact du rayonnement UV sur le cycle du sulfure
de dimťthyle (DMS) et du propionate de dimťthyle sulfonium (DMSP),
le principal prťcurseur du DMS, s'exerce ŗ diffťrents niveaux :
-
en inhibant
la croissance des organismes phytoplanctoniques possťdant du DMSP
-
en stimulant
l'accumulation de DMSP ŗ l'intťrieur des cellules phytoplanctoniques
-
en inhibant
la dťgradation bactťrienne du DMSP et du DMS
-
en dťgradant
photochimiquement le DMS
Les prymnesiophytes sont les principaux producteurs
du DMSP (Belviso et al., 2001). Les rťgions polaires, sub-polaires
et tempťrťes qui sont les plus touchťes par la diminution de la couche
d'ozone, et donc par une augmentation du flux d'UV-B, sont aussi le
siŤge d'efflorescences massives de prymnesiophytes tels que Phaeocystis sp.
et de Emilinia huxleyi. La grande sensibilitť de E. huxleyi au
stress UV-B a ťtť dťmontrťe au laboratoire (Buma et al., 2000 ; Garde
et Caillau, 2000). En inhibant la croissance des organismes phytoplanctoniques
possťdant du DMSP, l'augmentation du rayonnement UV-B devrait rťduire
la concentration du DMSP dans les eaux de surface.† Cependant,
Sunda et al. (2002) ont montrť que E. huxleyi pouvait augmenter
sa capacitť de synthŤse de DMSP en rťponse ŗ diffťrents stress oxydatifs† (forte
concentration en Cu2+, limitations en Fe ou en CO2,
exposition au rayonnement UV). Le DMSP agirait comme un agent antioxydant
permettant de neutraliser les composťs d'oxygŤne rťactifs gťnťrťs ŗ l'intťrieur
de la cellule par les diffťrents facteurs de stress oxydatifs. L'ťtude
de la rťponse due au stress UV montre que l'augmentation de la concentration
intracellulaire du DMSP n'est apparemment pas stimulťe par le rayonnement
UV-B mais plutŰt par le rayonnement UV-A (Sunda et al., 2002 ; van
Rijssel et Buma 2002). Ce rťsultat semble assez logique si on considŤre
que les photons des UV-A sont les principaux responsables des dommages
oxydatifs. La sensibilitť de la concentration de DMSP de surface ŗ une
augmentation du rayonnement UV-B dans les hautes et moyennes latitudes
serait donc d'autant plus grande du fait de l'absence d'effet compensatoire
au niveau de la physiologie des algues. Le DMSP constitue une source importante, voire essentielle,
de soufre pour les bactťries, mais ťgalement une source de carbone
non nťgligeable (Kiene et al., 2000). L'effet des UV-B sur la consommation
bactťrienne du DMSP en solution dans l'eau de mer est plutŰt faible
et rťsulterait, selon Slezak et al. (2001), de l'inhibition partielle
de l'activitť bactťrienne. Celui des UV-A est bien plus important (Slezak
et al., 2001). Enfin, en bout de chaÓne, la photolyse du DMS paraÓt
plus efficace dans le domaine des UV-A que celui des UV-B (Kieber et
al., 1996 ; Brugger et al., 1998). Cette photolyse s'effectue principalement
de maniŤre indirecte en prťsence de photosenbilisateurs (Brimblecombe
and Shooter, 1986) et l'importance du processus de photolyse augmente
avec celle de la concentration de MOD (Brugger et al.,1998).
Il semble donc que l'effet des UV-A sur les processus
de production et de destruction des composťs soufrťs du type DMSP et
DMS soit supťrieur ŗ celui des UV-B. En consťquence, les effets climatiques
sur les processus de photolyse et de dťgradation du DMSP par les bactťries
pourraient plus se poser en termes de changement du flux d'UV-A, liť ŗ la
nťbulositť, plutŰt que d'UV-B, liť ŗ la diminution de la couche d'ozone. |
|